Conviene hacer notar que, si bien los aldehídos y cetonas son los compuestos más sencillos con el grupo carbonilo, hay otros muchos compuestos que contienen también en su molécula el grupo carbonilo que, junto a otras agrupaciones atómicas, constituyen su grupo funcional característico. Entre estos compuestos podemos citar: ácidos carboxílicos, —CO—OH; halogenuros de acilo, —C—X, ésteres, —CO—OR, amidas, —CO—NH2 , etc., sin embargo, el nombre de compuestos carbonílicos suele utilizarse en sentido restringido para designar exclusivamente a los aldehídos y cetonas.
Nomenclatura
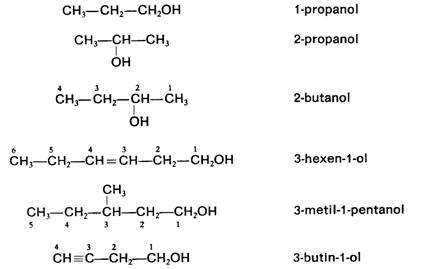
En la nomenclatura sistemática, los aldehídos se nombran cambiando por al la o terminal del nombre del hidrocarburo correspondiente a la cadena hidrocarbonada más larga que incluya el grupo funcional —CHO, al que se le asigna la posición 1 a efectos de enumerar los posibles sustituyentes. Los nombres de las cetonas se forman de manera análoga, pero cambiando por ona la o terminal del hidrocarburo progenitor e indicando, si es preciso, la posición del grupo —CO— con un número (el más bajo posible). Las cetonas suelen nombrarse también corrientemente mediante los nombres de los dos radicales unidos al grupo carbonilo, seguidos de la palabra cetona. Ejemplos:

Muchos aldehídos tienen nombres vulgares que derivan del nombre común del ácido carboxí1ico correspondiente, (formaldehído, acetaldehído, etc.).